

Epidémia COVID-19, ktorá nás zasiahla nevídaným spôsobom, nám okrem obmedzení a strachu priniesla do života aj množstvo informácií o epidemiológii, mikrobiológii a infektológii. Zorientovať sa v laboratórnych vyšetreniach na SARS CoV 2 môže byť dosť zložité.
Správna indikácia a interpretácia s ohľadom na ich limity má ďalekosiahle dosahy nielen na pacienta, ale aj na verejné zdravie. Indikácia nesprávneho testu a jeho falošne negatívny výsledok môžu stáť za novým ohniskom nákazy nielen v domácnostiach, ale najmä v zdravotníckych a sociálnych zariadeniach.
Základné vyšetrovacie metódy vo virológii možno najľahšie rozdeliť na:
V ére COVID-19 sa opierame o tri vyšetrovacie metodiky: detekciu nukleových kyselín vírusu (PCR), dôkaz antigénov a protilátkové testy. Nutnosť skorej diagnostiky COVID-19 preniesla diagnostiku z laboratórií do ambulancií lekára v omnoho väčšej miere ako doteraz. Rýchlotesty na diagnostiku SARS CoV2 (presnejšie bedside testy alebo Point-Of-Care testing, POCT) sú dostupné pre všetky z týchto metodík.
Pred podrobnejším popisom jednotlivých metodík je nutné spomenúť predanalytickú fázu testovania – odber materiálu. Aj najcitlivejšia metodika na svete, akou je PCR, nedokáže adekvátne vyšetriť vzorky s nedostatkom materiálu. Dostupné metodiky sú prispôsobené na analýzu materiálu z výteru z nosohltanu, prípadne kombinovaného výteru z nosohltanu a hrdla. Najvyšší záchyt vírusu sa popisuje v zostupnom rade z bronchoalveolárnej laváže hlienu (diagnostické bronchoskopické vyšetrenie – pozn. red.), výteru z nosohltana a s najnižším záchytom z výteru z hrdla. Vývoj testovania však upiera svoju pozornosť na sliny ako ľahko dostupný materiál s možnosťou samoodberu pacientom. Teraz však musíme realizovať odber za dodržania adekvátnej ochrany zdravotníka invazívnejším výterom. Výter pre RT-PCR vyšetrenie a antigénové testy je zatiaľ rovnako rizikový a je potrebné dodržať všetky zásady bezpečnosti s adekvátne použitými osobnými ochrannými prostriedkami.
Pri spracovaní vzoriek je nutné myslieť okrem bezpečnosti pacientov aj na vysokú senzitívnosť PCR vyšetrení: PCR je veľmi senzitívna metodika a vo vysokej miere je schopná zachytiť aj minimálne počty vírusov. Minimálna kontaminácia negatívnej vzorky môže viesť k záchytu falošnej pozitivity (nutná výmena rukavíc po každom odbere). (Obr. 1.)
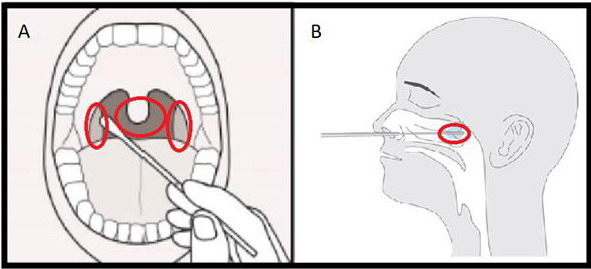
Polymerázová reťazová reakcia s reverznou transkripciou (RT-PCR)
Zlatým štandardom v diagnostike COVID-19 s vysokou senzitívnosťou už v skorých štádiách ochorenia je RT-PCR. Z výteru je nutné najprv izolovať RNA (ribonukleovú kyselinu). Táto špecifická genetická informácia vírusu (presnejšie dva až štyri špecifické gény SARS CoV 2) je následne pomocou enzýmov prepísaná do DNA, ktorá je následne v minimálne 40 cykloch rozmnožená (amplifikovaná). Na základe interakcie presne určenej DNA so špecifickými fluoreskujúcimi reagenciami vzniká svetelný signál, ktorý deteguje prístroj. Dostupné testy sú založené na detekcii génov E, N, S a RdRP, pričom za pozitívny výsledok možno hodnotiť len pozitivitu minimálne dvoch génov. Podľa niektorých indícií pomôže množstvo vírusu vo vzorke identifikovať takzvaných superšíriteľov. Prahový cyklus alebo Ct (angl. threshold cycle) je cyklus, v ktorom dochádza k záchytu svetelného signálu sledovanej RNA. Pri vysokom množstve vírusu vo vzorke dochádza k záchytu v nízkych cykloch amplifikácie, naopak v prípade pacientov s pretrvávajúcou pozitivitou PCR na SARS CoV 2 po prekonaní infekcie dochádza k záchytu DNA zväčša po 30. cykle. Výsledok každého vyšetrenia sa porovnáva s pozitívnou a negatívnou kontrolou. Samostatnú kontrolu má aj prítomnosť biologického materiálu na kontrolu adekvátnosti odberu pri každom vyšetrení.
Senzitívnosť vyšetrenia závisí od viacerých faktorov, ale najviac od štádia ochorenia, druhu výteru a jeho adekvátnosti. Početnosť falošne negatívnych výsledkov varíruje od dvoch až po 39 %. Je nutné dodať, že pri správne indikovanom (v správnom čase – chorý alebo po uplynutí inkubačnej doby po expozícii) a adekvátne realizovanom výtere (dôrazný kombinovaný výter z hrdla a nosa) je najpresnejším z dostupných testov. Najväčšou nevýhodou tejto metodiky je jej náročnosť, obmedzená kapacita laboratórií, cena a dostupnosť výsledkov laboratórneho vyšetrenia.
V segmente POC testov je priestor aj na PCR a náskok majú riešenia doteraz aplikované na diagnostiku chrípky. V dohľadnej dobe možno pravdepodobne očakávať dve metodiky poskytujúce tzv. sample-to-answer system – od vzorky priamo k odpovedi bez laboratória. V dlhšom horizonte bude na trhu omnoho väčšia ponuka s ohľadom na 104 EUA povolení od FDA na tieto druhy testov (7/20). Nepredpokladám možnosť plošného používania týchto testov, avšak budú nenahraditeľné v emergentných situáciách (ARDS, polytrauma, transplantačný program, atď.).
RT PCR testy – účelom testu je potvrdenie prítomnosti vírusu u jedinca aj s minimálnym množstvom vírusu. Identifikácia SARS CoV 2 pozitívnych jedincov vrátane asymptomatických na začiatku ochorenia.
Ide o „zlatý štandard“ laboratórnej diagnostiky COVID-19.
Výhody: Vysoká citlivosť a presnosť.
Nevýhody: Náročnosť, cena, obmedzená kapacita laboratórií, dostupnosť výsledkov, možnosť kontaminácie.
Antigénové testy
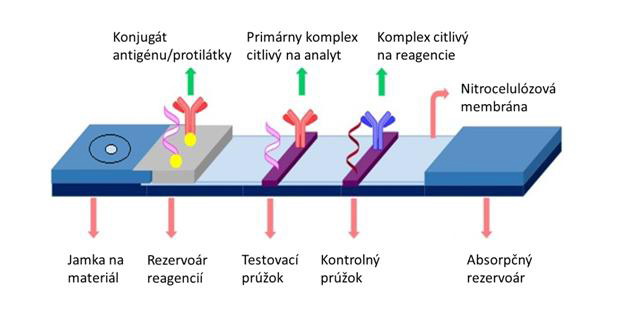
Veľmi horúcou novinkou v diagnostike SARS CoV 2 sú antigénové testy. Antigény sú z chemického pohľadu veľmi heterogénna skupina zlúčenín, ktoré spolu tvoria vírusové častice. Pri diagnostike COVID-19 testujeme prítomnosť nukleokapsidového proteínu. V laboratóriách testujeme antigény metódou ELISA (enzyme-linked immuno sorbent assay) avšak pri COVID-19 sa dôraz kladie na POC testy využívajúce technológiu Lateral Flow ImmunoAssay (LFIA). Je to imunochromatografická technika pozdĺžneho toku reagencií prúžkom poréznej membrány, ktorú sme doteraz najviac používali pri tzv. baby testoch. LFIA využívame aj pri POC testoch protilátok. Najväčšou výhodou týchto testov je dostupnosť výsledkov v priebehu niekoľkých minút (zväčša 15). (Obr. 2.)
Test je vytvorený na diagnostiku chorých príznakových pacientov s COVID-19 najmä na začiatku ochorenia. V tomto období telo tvorí najväčšie množstvá vírusu a citlivosť testov je veľmi vysoká, podľa druhu testu až do 97 %. Pri nízkej vírusovej náloži klesá senzitívnosť testu. Nízku vírusovú nálož evidujeme na začiatku ochorenia v inkubačnej dobe a v rekonvalescencii. Antigénové testy nie sú schopné zachytiť antigény vírusu pri nízkej vírusovej náloži, ktorá zodpovedá prahovým cyklom RT-PCR nad 30. Doteraz neexistuje jednoznačný vedecký názor, ktorý by stanovoval riziko prenosu infekcie podľa množstva vírusu pri vyšetrení. Určenie tejto hranice modifikuje množstvo faktorov (detekčná hranica PCR metodiky, adekvátnosť odberu, mechanizmus prenosu, atď.), avšak existujú indície, že CT nad 30 je hranicou, pri ktorej je prenos infekcie významne obmedzený, napríklad dôraz na dohľadávanie kontaktov v Japonsku podľa Ct PCR alebo nízka schopnosť infikovať bunkové kultúry zo vzoriek s takto vysokým CT.
V klinickej praxi denno-denne zachytávame antigén pozitívnych pacientov bez príznakov po kontakte s COVID-19. Zväčša udávajú len mierne ťažkosti pripisujúce vyčerpaniu z práce, a tak si vo väčšine prípadov neuvedomujú epidemiologické riziká.
Antigénový test – rýchla identifikácia pacientov s respiračnými príznakmi
Výhody: Rýchla dostupnosť výsledku, vysoká presnosť pri symptomatickom jedincovi, cena, bez nutnosti prístrojového vybavenia.
Nevýhody: Malá citlivosť pri nízkej vírusovej náloži v prípade bezpríznakových jedincov (po 30. prahovom cykle PCR).
Sérologické vyšetrenie protilátok
Najčastejšími mikrobiologickými vyšetreniami vírusových ochorení bolo donedávna najmä vyšetrenie protilátok s ohľadom na vybavenosť mikrobiologických laboratórií a iné okolnosti. Pri testovaní SARS CoV 2 sme pod obrovským časovým stresom, čo neumožňuje pri identifikácii nakazeného čakať na imunologickú reakciu. Pri COVID-19 dochádza k tvorbe IgM protilátok v rozmedzí jedného až 14 dní a IgG zväčša po dvoch týždňoch. Množia sa tiež počty pacientov, ktorým sa protilátky netvoria vôbec napriek prekonaniu aj symptomatickej infekcie. Z tohto dôvodu nám stanovenie protilátok vo väčšine prípadov povie len to, či človek prekonal infekciu, poprípade v akom čase. Dôležitou je dnes aj otázka množstva neutralizačných protilátok v krvi s ohľadom na očkovanie alebo určenie vhodného darcu konvalescentnej plazmy. Z pohľadu určenia ďalšieho postupu pacienta s COVID-19 nám prítomnosť protilátok triedy IgG umožňuje spolu s informáciami o úplnom ústupe klinických príznakov v rozmedzí desiatich až 20 dní od záchytu SARS CoV 2 ukončiť karanténu.
Laboratórne vyšetrenie protilátok sa realizuje prevažne na dvoch platformách, a to ELISA (enzyme-linked immuno sorbent assay) a ECLIA (electrochemiluminescence immunoassay). Obe metodiky využívajú väzbu antigénu a protilátky.
Protilátkové rýchlotesty fungujú rovnako na princípe Lateral flow immunoassay. Dorazili k nám na Slovensko s prvými zásobami OOP z Číny. Dovoľujeme si však povedať, že vzhľadom na priskorú indikáciu spôsobili viac komplikácií ako osohu. Nemožno ich použiť na identifikáciu akútne chorých.
Protilátkové testy – informácia o imunitnej reakcii po prekonaní infekcie COVID-19
Výhody: Cena, rýchla dostupnosť výsledkov.
Nevýhody: Absolútne nepoužiteľné na identifikáciu infikovaných pacientov.
Pre správnu indikáciu jednotlivých testov je nutné si uvedomiť, že priemerná inkubačná doba COVID-19 je štyri až päť dní. Skoršia indikácia nielen antigénového testu, ale aj PCR vyšetrenia bude viesť k negatívnemu výsledku aj v prípade nakazenej osoby bez príznakov. V prípade osôb s PCR potvrdenou infekciou SARS CoV 2 nie je potrebné opakovanie PCR testu. O ukončení karantény rozhoduje klinický obraz ochorenia, nie PCR test.
Autori: MUDr. Martin Novotný, PhD., MUDr. Ondrej Zahornacký